暨南大学药学院考研——氧化反应
常用氧化剂有KMnO4 、浓HNO3 、K2Cr2O7+H2SO4 、CrO3+HOAc 、
CrO3+ 乙酐、CrO3+ 吡啶、CH3COCH3+Al(OCHMe2)3 、HIO4 、MnO2 、H2O2、RCO3H(有机过氧酸)、Tollen’s、Fehling’s、Br2水、空气氧化、臭氧化……
1、KMnO4氧化
【特点】氧化性强,通用。
例

2、铬酸氧化
(1) K2Cr2O7+H2SO4
【特点】通用氧化剂,氧化性强。
例

用K2Cr2O7+H2SO4氧化仲醇,速度快、产率高。是由仲醇制备酮的好办法。

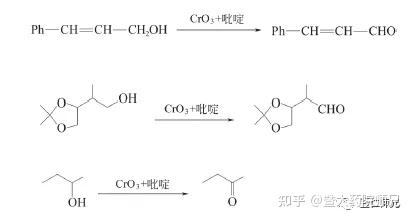
(2) (CrO3+吡啶)氧化
这类氧化剂包括PCC、PDC和Sarett试剂。PCC(氯铬酸吡啶盐pyridinium
chlorochromate,C5H5NH+CrO3Cl-)是吡啶和CrO3在盐酸溶液中的配合盐,橙红色晶体;PDC[重铬酸吡啶盐 pyridinium dichromate,(C5H5NH)2
2+Cr2O72−]是将吡啶加入到三氧化铬的水溶液中而形成的亮黄色固体;Sarett试剂是三氧化铬⁃双吡啶配合物[(C5H5N)2·CrO3]。它们在DCM(二氯甲烷)中有一定的溶解度,使用很方便,在室温下便可将醇氧化为醛或酮,而且基本上不发生进一步的氧化作用、不氧化C C。其中PDC的氧化性略强于PCC,在DMF(N,N⁃二甲基甲酰胺)中可将伯醇氧化为酸。
【特点】适宜氧化醇→醛、酮。产物专一性好,不氧化双键,对分子其他部分影响极小。
例
(3)CrO3+乙酐

3、丙酮+异丙醇铝氧化(Oppenauer氧化)
又称为Oppenauer氧化,其特点是可氧化羟基为羰基,但不氧化双键,特别
适合将不饱和仲醇氧化为相应的不饱和酮。


4、HIO4氧化
氧化邻二醇,发生碳碳键的断裂,生成醛或酮。

5、MnO2氧化
新生的MnO2氧化性较温和,不氧化双键。

6、H2O2及过氧酸氧化
(1)氧化双键

(2)氧化酮——Baeyer⁃Villiger氧化
有机过氧酸与酮反应,生成酯。因反应过程中碳胳发生变化,又称为
Baeyer⁃Villiger重排。

迁移优先次序:叔烷基>仲烷基>环己基>苄基>苯基>伯烷基>甲基。
立体化学:迁移过程不改变R'的立体构型。

7、Tollen’s及Fehling’s氧化
【特点】 弱氧化剂,将醛基氧化成羧基,均不氧化双键。
【区别】 Tollen’s(硝酸银的氨溶液)——氧化所有的醛;
Fehling’s(硫酸铜与酒石酸钾钠的混合液)——只氧化脂肪醛,不氧化芳香
醛。
8、溴水氧化(考试重点)
弱氧化剂,只氧化醛糖,不氧化酮糖。

9、空气氧化
空气氧化的产物取决于催化剂和反应物结构。

文章被以下专栏收录


