有机化学知识点整理——烯烃部分
烯烃部分知识点纲要
2020.3.20修改
增加烯烃部分思维导图,修改一些排列,增加目录链接
这里插一句,如果有问题可以私信问我,如果觉得不好意思打扰,可以象征性地付一块钱咨询吧哈哈哈。
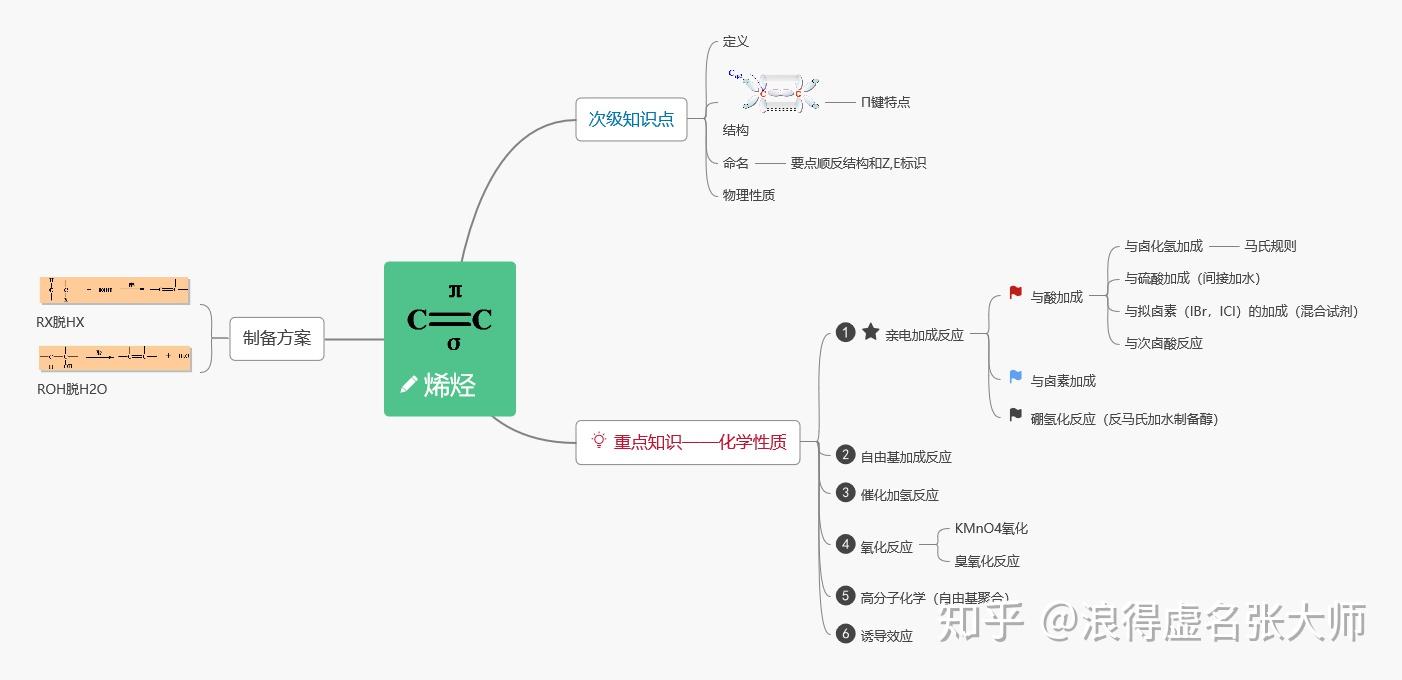
知识点纲要(图片来源:chemdraw手绘、百度百科、百度文库ppt)参考书籍《有机化学学习指导》东南大学出版社
链接百度百科知识点
有机化学的学习存在困难,大多数情况是不知道如何记忆,我觉得理清思路和逻辑,在这个基础上学习,可能效果会很好。这个就是一个大体的框架和思路的概念,在这个基础上还要通过书本来丰富内容。
专栏目录链接
次级知识点
- 定义
分子种含有碳碳双键的不饱和烃,通式为CnH2n.
烯烃的同分异构除了碳链异构还有官能团位置异构。
- 结构
烯烃种双键碳原子采用sp2杂化,一个双键种包含一个σ键和一个Π键。
Π键的特点:重叠程度小,容易断裂,性质活泼。受到限制,不能自由旋转,否则Π键断裂。
(反应依据)
- 烯烃的命名
要点:顺、反结构:碳碳双键不能旋转而导致烯烃分子中原子或基团在空间的排列形式不同。当双键碳中有一个碳原子上连有两个相同的原子或原子团时,不存在顺反异构。
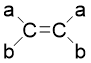
顺式
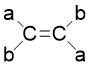
反式
Z,E标记结构:当双键碳上连有4个不同的原子或原子团时。如果两个优先基团处于双键的同一侧,则为Z式构型,在异侧,则为E。
- 物理性质
- 状态
- 熔沸点、相对密度
- 注意点:顺式异构体的熔点比反式异构低,因为反式异构体具有更高的对称性。
顺式异构体的沸点比反式异构高,因为顺式异构体具有偶极矩,分子间存在偶极之间的作用力,反式异构体不存在偶极矩。
重要知识点
烯烃的化学性质
- 第一部分:Π键重叠程度低,易发生断裂。Π键因为有2个电子,可以看成是Lewis碱.Π键很容易受到缺电子物质Lewis酸的进攻而发生断裂而发生亲电加成反应。
亲电加成反应
- 与酸的加成
(1)与卤化氢的加成

机理:

亲电加成反应的活性
酸的酸性越强,越容易与烯烃反应,故卤化氢活泼性次序为:HI>HBr>HCl
烯烃双键上的电子云密度越高,亲电加成反应的活性越高。
不对称烯烃与卤化氢加成:不对称烯烃与卤化氢加成遵循马氏规则:氢原子加在含氢较多的碳上,卤原子加在含氢较少的碳上。

马氏规则的理论解释:碳正离子稳定性
马氏规则

碳正离子生成速度是决速步骤,而稳定性:仲C+>伯C+,仲C+较易生成,从而仲卤代烃生成速度快,是主要产物。
碳正离子的重排

碳正离子重排:2°→3°(更稳定)

注意:
同样有负氢重排(H-)
SN1,E1反应中也有重排现象,因其经历碳正离子中间体
(2)与硫酸的加成(间接加水)
烯烃能与浓硫酸反应,生成硫酸氢烷酯。硫酸氢烷酯易溶于硫酸,用水稀释后水解生成醇。
工业上用这种方法合成醇,称为烯烃间接水合法。

不对称烯烃与硫酸加成也遵守马氏规则。
(3)与拟卤素ICl、IBr的加成(混合试剂)
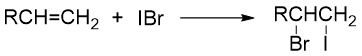
(4)与次卤酸的反应
烯烃与次卤酸加成,生成β-卤代醇。由于次卤酸不稳定,常用烯烃与卤素的水溶液反应。

- 与卤素加成

附加:溴的四氯化碳溶液与烯烃加成时,溴的颜色会消失,可用来鉴别烯烃。
卤素活性:氟>氯>溴>碘


环状溴鎓离子(cyclic bromonium ion)历程—解释立体化学事实
- 硼氢化反应(hydroboration)反马氏加水制备醇
不对称烯烃与乙硼烷加成后再经过氧化氢碱性水解得到反马氏规则产物。


第二部分:自由基加成反应(过氧化效应)
当有过氧化物存在时,烯烃与溴化氢发生的不是离子型的亲电加成反应,而是自由基加成反应。加成的反应取向是反马氏规则,但对HCl、HI加成反应的取向没有影响。
反马氏规则


第三部分:催化加氢反应和氢化热
常用催化剂:Ni,Pt,Pd等
机理:异相催化,顺式加成。

1mol的烯烃打开双键生成烷烃所放出的热量称为氢化热。氢化热越小,烯烃的稳定性越大。反式烯烃稳定性大于顺式,取代基越多的烯烃越稳定。
第四部分:氧化反应(根据生成物的结构可推断烯烃的结构)
- (检验烯烃)高锰酸钾氧化
在中性或碱性介质中高锰酸钾可以将烯烃氧化为邻二醇。
在酸性介质中高锰酸钾可以将烯烃氧化成羧酸、酮和二氧化碳,紫色消失。

- 臭氧化反应
烯烃在5%左右的臭氧中氧化,再经过金属锌还原,产物为醛或者酮。

第五部分:(高分子化学的重点知识)自由基聚合

机理

六、诱导效应
1、定义:在有机化合物分子中,由于电负性不同的取代基(原子或原子团)的影响,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应,叫诱导效应。
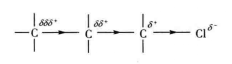
2、特征:
a)近程性:沿着碳链传递,并随着碳链的增长迅速减弱或减少。
b)永久性:通过静电诱导而影响到分子的其他部分,没有外界电场的影响也存在。
3、形式:有吸电子诱导(-I)效应和给电子诱导(+I)效应,C-H键的诱导效应规定为零。
4、取代基的诱导效应强弱有如下规律:
同族元素中,原子序数越大,吸电子诱导效应越弱;同周期元素中,原子序数越大,吸电子诱导效应越强。
基团不饱和程度越大,吸电子诱导效应越强。这是由于各杂化态中s轨道成分不同而引起的,s成分越高,吸电子能力越强。
正电荷基团和含配位键(直接相连)的基团具吸电子诱导效应,负电荷基团具给电子诱导效应。
烷基具给电子诱导效应和给电子超共轭效应。
烯烃的制备
- RX脱HX

- ROH脱H2O

文章被以下专栏收录


